Föreläsare: Undersköterska Stig-Göran Wiklund, Centrallasarettet Västerås
 Stig-Göran Wiklund kommer ursprungligen från svenska Österbotten i Finland, Vasa närmare bestämt.
Stig-Göran Wiklund kommer ursprungligen från svenska Österbotten i Finland, Vasa närmare bestämt.
1976 gick han sin första egentliga sjukvårdsutbildning vid Vasa sjukvårdsläroanstalt. En utbildning som kallades Medikalvaktmästare/ Ambulansförare och som uppfanns för att få in killar i vården i Finland.
Efter fullbordad Militärtjänst åkte Stig-Göran över till Sverige och Västerås där han fick jobb inom 5 dagar. Hans första jobb blev sjukvårdsbiträde i poolen, men ganska snart kom han över i Klinikbunden pool på IVA, ett vikariat som senare övergick i ordinarie tjänst.
Stig-Görans jobb på IVA i dag är att jobba som underskötare med speciellt ansvar för Respiratorer. Han undervisar också i praktisk respiratorkunskap och deltar i utformning av kursmaterial och tester av personalens kunskaper på området. Detta är ett ständigt pågående utvecklings arbete.
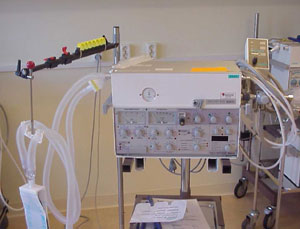
Respiratorhistorien började på 1950-talet , varför jag tänkte börja berätta om den här gamla respiratorn ”Engström”, som fanns i bruk även när jag började 1977. Den första respiratorn som slog igenom ”riktigt stort” var ”Engström 150”. Det var egentligen två respiratorer, invasiv ventilation och non-invasiv ventilation, den s k järnlungan.
Järnlungan var en väst av plåt som man satte runt överkroppen och som slöt tätt runt hals, armar och mage. Därefter lade man ned en gummitub med en liten syrgas-näsa på och sprutade syrgas. När man sedan sög vakuum i den här västen vidgades bröstkorgen och luft gick ner i lungan. Detta var egentligen mycket bra lungmässigt sett. Det som hände var att det blev i stort sett samma tryckförhållanden som när man andades normalt själv. När vi andas normalt själva blir det lätt vakuum när vi drar in andetaget och ett lätt övertryck när vi andas ut. Det skulle ha varit mycket bra om det hade fungerat även på våra patienter, men de var ju sjuka och de svettades och de behövde tvättas. Det blev ett instängt område och då blev man tvungen handventilera medan man tvättade patienten. Det gick inte hygienmässigt, det blev trycksår runt armar och hals och buk. Man kunde inte heller kontrollera tillfredsställande.
Däremot invasiv ventilation när man stoppade ned en tub med kuff, som slöt tätt, och pressade luft med våld fick man bättre kontroll och visste exakt hur mycket man blåste in och kunde mäta allt som kom ut. På den tiden var man inte så rädd för höga tryck i lungorna. Däremot var man mycket rädd för 100% syrgas. Det är vävnadsdödande och direkt farligt, varför man försökte hålla nere syrgasprocenten men lade på ordentligt med luftvägstryck. Jag minns när jag började 1977 att det var vanligt att patienter låg med 50-60cmH2O i luftvägstryck, tillfälligt ännu högre. Idag förekommer inte det. Vi tycker patienterna har höga luftvägstryck om de ligger på 30-35cmH2O. Hela respiratorvården idag strävar efter att ge varje andetag lägsta möjliga luftvägstryck. Vi har lärt oss att de höga luftvägstrycken sliter sönder lungparenchymen så att man får en stor traumatisk skada i lungorna. Idag har vi sådana apparater att vi med olika medel kan ge andetaget lägsta möjliga tryck.
Alla de här första respiratorerna som kom var volymkontrollerade, vilket betyder att man ställer in en volym, ställer in frekvensen och pressar ned. Om man har en svårt lungsjuk patient med obstruktiva lungor får man höga luftvägstryck. Men har man en patient som är ganska frisk i sin lungor och har mjuka eftergivliga lungor får man ett lägre luftvägstryck. Ibland hade man höga luftvägstryck och hur gjorde vi då för att få ned trycket? Då kunde man ändra på tiden. Ett normalt andetag har ett inspirations- och expirationsförhållande i tid på 1 till 2, en del inandning och två delar utandning. Det beror på att när jag andas in skerdet aktivt och passivt då bara släpper man, det senare tar dubbelt så lång tid. Det är det normala andningssättet. Vad man kunde göra då vid höga luftvägstryck var att manipulera med de här tiderna så att man förlängde inandningstiden. Man kunde t ex köra på ett förhållande 1 till 1, man förlängde inandningstiden så att den blev lika lång som utandningstiden. Om man hade ett bestämt andetag som man gav på en längre tid blev det lägre flödeshastighet och därmed ett lägre luftvägstryck. På det sättet kom man undan de höga luftvägstrycken. Det gör vi än idag, men vi har mera sofistikerade metoder.
Den här gamla Engström-respiratorn var uppbyggd av ett maskinsystem och ett patientsystem. När man skulle lära ut hanteringen av respirator på den tiden så var det enkelt. Maskinsystemet innehöll delar av god kvalitet som höll. När de här respiratormodellerna hade tjänat ut skickade vi dem till Polen och de har säkert ”tuffat och gått” ända fram till dessa dagar. Maskinsystemet bestod av en ASEA-motor, en växellåda och en kolv som gick fram och tillbaka i en cylinder och bildade ett övertryck och ett undertryck. Detta skickades upp i tryckkammaren, patientsystemet. I tryckkammaren hängde en gummiblåsa och med hjälp av en ratt ställde man in hur mycket luft man skulle ge patienten. Syrgashalten ställdes in med flödesmanometrarna. Det fanns tabeller som angav rätt syrgasprocent. Under- och övertrycket kom nedifrån maskinsystemet och när det blev vakuum i behållaren sögs blåsan ut och då gick den syrgas och luft in som vi hade ställt in. När kolven kom tillbaks blev det övertryck, då pressades blåsan ihop och luften gick ut till patienten. Så enkelt var det.
Det fanns två manometrar, luftvägstrycksmätaren, där vi mätte motstånd, hur tungt det var att blåsa in luft till patienten. Det hette på den tiden insufflationstryck, på 1980-talet hette den luftvägstryck och sedan 1990-talet kallas det topptryck. Det är olika uttryck för samma sak.
Minutvolymen var viktig. Vi hade ställt in en viss volym som vi ville ha in per minut, vilket kunde mätas med en spirometer. Man växlade på ett vrede och kunde släppa på luft till spirometern och mätte under en minut. Så knuffades den fram för varje andetag och man kunde avläsa hur många liter per minut man gav patienten. Man ställde in frekvensen, man ställde in arbetsflödena, arbetstrycken med hjälp av rattar.
Befuktning var ett sorgligt kapitel på den här tiden. Vi hade aktiv befuktning som egentligen var värdelös, då vi inte hade förstått att för att kunna behålla fukten i luften måste man hålla den varm hela vägen in till patienten. Först hade vi befuktningsbehållaren som innehöll 1%-ig Hibetan som stod dygn efter dygn och luften passerade behållaren och gav en befuktad luft. En del dunstade. Förutom det hade vi en liten elektrisk platta som var kokhet och dessutom ett sterilvattendropp som droppade sterilvatten på den här plattan. Det sade puff, puff, puff för varje gång och det dimmades sönder till fuktig dimma. Det var ju bara det att vi lät det kallna på väg till patienten. Vi hade således vätskefällor på slangarna som vi tömde varje timme. Om vi lade in en och en halv liter sterilt vatten per dygn i befuktaren tömde vi ca 1,3 liter i vattenfällorna. Det var inte mycket patienten fick. Idag har vi mycket bättre befuktning. Som tur var var inte patienterna lika sjuka som de är idag. De patienter som vi då lade in respirator skulle vara alltför friska för att komma till intensivvårdsavdelningen idag. De patienter vi har idag är mycket sjuka och har ofta multipla sjukdomar.
Vi hade ett avtorkningsfilter, blå gel. Respiratorn kunde skadas om fukt kom in i respiratorn. Man hade en liten burk med blå gel dit all utandningsluft gick. Den lilla fukt som passerade patienten och gick ut i utandningsslangen via filtret färgade filtret rosa. När det var rosa var det mättat med fukt. Varje dygn bytte man det där blå gelet. Under 1950- och 60-talen kokade man det blå gelet och kokade det så att det blev blått igen och kunde återanvändas. Under min tid hade man jättestora blå gelsburkar som vi bara öste ur och vartefter det blev rosa kastade vi och lade in nytt för att torka den här luften som gick tillbaka till respiratorn.
Rengöringen var ett kapitel för sig. Alla gummislangar lades i Hibitan-lösning eller klorhexidinlösning en timma. Dessutom fanns det en mängd metallkopplingar som inte gick att ta loss. Enda sättet för att rengöra dessa metallkopplingar var att packa spritkompresser. Vi packade spritkompresser i alla håligheter på respiratorn och sedan fick det stå en timma. Sedan gjorde vi odling på en tio till tolv olika ställen. Jag har en historia från den tiden. När jag började med det här odlade jag de här respiratorerna och när man odlade dessa respiratorer skickades odlingarna till bakteriologiska laboratoriet och fick vänta nästan en vecka innan man fick svaren. Man fick inte använda respiratorn förrän man fått svaret att den var ren. Vi hade åtta respiratorer, fyra som gick och fyra som väntade på klartecken från bakt lab. När jag började med det här växte varenda en. Så snart jag odlade dem så växte de. Den gamla undersköterskan vi hade blev bara argare och argare för varje vecka. Jag fick ju göra om odlingarna med nya spritkompresser. Vi blötlade på nytt och gjorde en ny provtagning och det blev samma sak igen. En dag tog hon mig i nacken och skulle lära mig hur man gjorde när man odla. Då var det på det viset att man fick inte odla på andra platser än där man hade haft spritkompresser. Därefter slutade det växa för mig också. Den var inte enkel att andas i. Jag har provat att andas i den här respiratorn och då var jag ung och stark och frisk. Det fanns en ventil som alltid skulle stå på ”open”. Om den stod på open kunde patienten dra egna andetag och det var inte lätt för våra sjuka patienter. Urträningen på Engströmsrespiratorns tid gick till så att när patienten hade legat några veckor i respirator och skulle börja urtränas väckte man patienten och sade att han skulle andas själv, varefter man kopplade ur fem minuter varje timme. När man hade legat och förlita sig på respiratorn i många dagar blev det en trygghet och när man skulle börja träna upp de dåliga andningsmusklerna själv fick patienten ofta panikångest. Patienten var vaken och tittade på klockan och visste att när det var fem minuter kvar ”då kommer de” och skall koppla ur. När vi kom och skulle koppla ur hade de ganska hög andningsfrekvens och pulsen högre än vanligt. Sedan fick de kämpa och andas i fem minuter och om det misslyckades lades de tillbaka i respirator. Vi försökte lugna dem så gott det gick. Vi hade ofta problem att träna ur patienterna från respiratorn.
På 1970-talet kom IMW-birden. Det var den första respiratorn som hade en form av urträning, man kunde alltså lätt själv dra egna extra andetag. Vi har tyvärr skrotat dem varför jag inte har någon bild på den och det finns inte idag på lasarettet. Samtliga dessa respiratorer är bortkastade. Det var en mycket enkel respirator som vår engelske chef Peter Lee skaffade till oss. Den gick inte på el utan på luft och syrgas. Man kunde alltså strypa luftströmmen ett antal gånger. Man tittade på patienten hur stora andetag man skulle ge. Det fanns tre rattar som var inbördes beroende av varandra där man ställde in flöde, volym och frekvens. Så snart man rörde en så var man tvungen röra de andra också.
När vi fick IMW-birden blev det mycket bättre. När de behövde kontrollerad andning låg de i gamla Engströmarn och när de skulle tränas ur lade vi dem i IMW-birden och det gick mycket bättre. IMW-birden var bra. Den hade också en aktiv befuktning, en liten plastbehållare med en kula och det sprutade sterilt vatten med högt tryck mot den här kulan så att det blev en befuktad dimma av luften. Det var kanske bättre än befuktningarna på ”Engströmarn” , men den var inte bra.
Nyheten på IMW-birden var att den hade en 02 mixer. På de gamla respiratorerna justerade vi syrgasen tillsammans med luften och gick efter en tabell, men på IMW-birden fanns det alltså en 02 mixer, man ställde bara in på 40% syrgas direkt. Nytt var också ”peep”. Peep är ett övertrycksandningssystem och som uppfanns 1967. Det är en av de största revolutioner som skett inom respiratorvården. Det blev t ex lättare att rädda personer vid drunkningsolyckor. Lungan är en behållare och om man drar in vatten i lungan och låter lungan falla ihop blir behållaren mindre och då kan vattnet sprida sig till friska alveoler och så småningom kladda igen en lunga. Har man ett peep, ett positivt expiratoriskt pressure, låter man inte lungan falla ihop utan man ger ett andetag och så har man kvar ett positivt tryck. När den allra första peep-ventilen tillverkades tog man från utandningssidan på respiratorn en gummislang och ledde ner i en vattentunna, 15 cm under vattenivån och har då 15 cm vattenpeep. Då måste man pressa ut luften mot det här mottrycket. Detta gjorde att man kunde hålla lungorna lite uppblåsta och fick en större lunga att ventilera samt att man hade det positiva trycket som låg på lungan hela tiden och förhindrade lungan att kladda ihop, vilket den gör vid en drunkningsolycka. Man kunde således bibehålla de alveoler som var öppna och kontentan efter tre dygn blev att man hade större lunga att ventilera innan man började. Man kunde också börja trycka tillbaka lungödemen, man kunde rädda förtidigt födda barn som inte har utvecklat surfactant. Det är ett ämne som håller alveolerna utspända. Förtidigt födda barn har outvecklade lungor som gärna vill kladda igen men med det här positiva sluttrycket kunde man spänna ut lungorna och ventilera.
Idag använder vi det på många andra sätt. För våra patienter som legat länge i respirator och har dålig andningsmuskulatur har vi något som kallas terapeutiskt peep, ett mycket lågt peep +2 till +4-5 cm vatten. När vi tränar ur patienterna har vi det här låga peep:et på. Vi dilaterar deras andningsapparat. Det är lättare att spontanandas med färdigdilaterade andningsrör än att både dilatera och dra själv. Vi kan idag börja träna ur dem tidigare ur respirator tack vare det här peep:et. Vi använder det nästan jämt, vid riktigt svåra lunginflammationer, vid KOL- sjukdomar etc. och kan därmed rädda många tack vare att vi har ett ganska högt peep i inledningsskedet, i krissituationen.
Man lade alltså till en extra peep på ”Engströmarn” och även IMW-birden fick peep när den kom.
1980 kom första ”Erican”.
Det var Engström som utvecklade en respirator som var modern. Det var en revolution när det gällde rengöring. För det första var den abstrakt, det var en mängd knappar. Jag som skulle lära folk sköta en respirator jag fick problem. Hur skulle jag lära ut när jag inte kunde visa på den gamla ASEA-motorn och växellådan och kolven som gick fram och tillbaka. Nu var det bara en fyrkantig låda med en massa knappar som blinkade. Vi lärde oss till slut. Den här tiden kom också larmen. De sista åren vi använde Engströmarn fick vi trycklarm och sista åren vi hade IMW-birden fick vi trycklarm. Men närjag började 1977 fanns inga trycklarm. När den gamla Engströmarn läckte gick man med ögonen längs alla slangar, eftersom ögonen är det känsligaste organ man har på kroppen. Man kände direkt när det läckte någonstans. Vi smorde med silikonfett när det läckte. Det gjorde vi på gamla Engströmarn och det gjorde vi på IMW-birden. Idag har vi mätmetoder och respiratorn ”skriker” så fort det läcker. Vi var inte vana vid larm så vi ställde larmgränsen alldeles för snävt vilket fick till följd att det larmade och tjöt hela tiden så snart patienten rörde sig. Personalen fick huvudvärk och vi pratade på avdelningsmötena om möjligheten att stänga av de här larmen, då de var mer till elände än nytta. Orsaken var dock den att vi hade inte förstått att man skulle ställa larmgränsen så att det larmade när det behövdes och inte i tid och otid. När vi kom på att vi skulle ställa larmgränsen lite vidare blev även Erica tyst och larmade bara när det behövdes. Då var verkligen larmen en hjälp.
Vad som var nytt med den här respiratorn var SIMW-funktionen (Synkroniserad intermittent mandatory ventilation). SIMW fungerar så att i de kontrollerade andetagen, volymkontroll, där bestämde vi frekvensen, volymen och så fick vi trycket. Men med SIMW garanterar vi t ex åtta andetag per minut och vi bestämde att vi ger ett andetag här och ett där för att det skall bli åtta per minut. Om patienten inte vill ha åtta, utan trigga, då flyttade respiratorn sin tidscykel och synkroniserade andetagen ihop med patienten. Patienten kände då att han behövde inte ställa in sig efter apparaten utan apparaten ställer in sig efter patienten. Detta minskade ångesten vid urträningen när han patienten kände att han fick bestämma. Inte nog med det, förutom de SIMW-synkroniserade andetagen kunde vi alltså ge inandningshjälp på de spontana andetagen och då blev det något helt annat. Vi kunde kontrollera och ge en viss garanterad del som vi visste att det här får patienten, sedan fick patienten sköta den spontana delen själv. Om han var för svag att dra de spontana andetagen gav det här inandningshjälp så att han kom upp i adekvata volymen så att han fick tillräckligt stora andetag. Därmed kunde patienten sköta en större del själv och man kunde börja plocka ner de ordinarie kontrollerade andetagen och låta honom ta över mera själv tills han andades spontant med inandningshjälp. Till sist andades patienten blandad syrgas och luft genom respiratorn men helt och hållet själv. Det var meningen att det skulle gå till på det sättet men det går lite snabbare i verkligheten. Man kör kontrollerat, på SIMW med inandningshjälp och sedan börjar man dra ner och när man märker att det börjar går bra kopplar man ur. Oftast kunde de här respiratorerna också reta patienten så att det fungerade väldigt dåligt. Vissa patienter kopplade man bara bort och lade på en näsa och då kände sig patienten fri och andades själv och då fungerade det mycket bättre. Han kände i alla fall att han behövde anpassa sig lite efter apparaten eller blev stressad av apparaten. Det finns många varianter.
Erikan var bra och Erikan har vi kört med ända tills förra året (2002), när den kastades ut. Vad som var revolutionerande med rengöringen var att här kunde man ta ut patientdelen (en plåtburk). Man slet sönder den i fem delar, slängde in den i diskmaskin, gick ut i apparatrummet och hämtade en ny torr, lade in den och täthetstestade. Tio minuter efter att vi hade tagit ut den från en patient kunde vi starta den på nästa patient.
Alla våra respiratorer har namn från djungelboken, Walt Disney etc, Så snart det kommer ut en ny film och vi köper en ny respirator så ger vi respiratorn ett sådant namn. Det är inte enbart barnsligt, det finns en verklighet bakom. Vi hade en liten kille som vaknade upp i respirator och när han hörde det här larmet på respiratorn, ett ljud han hörde varje gång vi sög slem, förknippade han det med ett fruktansvärt obehag. Var livrädd för respiratorn. Varje gång han hörde pipet kröp han upp i sängen. Det var en klok person som sade att ”Vet du inte att den här apparaten heter Kalle?”. ”Heter den Kalle?”. ”Ja, Kalle som i Kalle Anka”. På en gång blev det något helt annat. När mormor och morfar och farmor och farfar kom på besök var det första killen sa att ”vet ni om att jag har legat i den här apparaten och den heter Kalle”. I denna abstrakta värld för ett litet barn är det viktigt om respiratorn heter Knatte, Fnatte eller liknande, då hittar det här barnet en sak som han känner till i den här miljön. Det blir då mycket varmare produkt än den fyrkantiga lådan som skriker och som gör ont varje gång vi suger slem. Vi har haft nytta av det några gånger när vi haft små barn. Det blir mäkta förvånade över att vi har en respirator som heter Kalle, vi har nu en respirator som heter Harry Potter. Barnen känner igen sig i namnet och kan börja prata runt namnet osv.
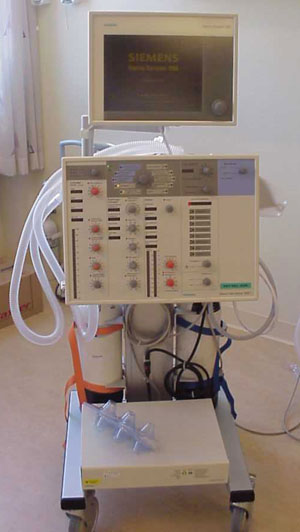
År 1984-85 köpte vi tre Servo 900C.
Orsaken var att vi ville åt ett nytt andningsmod som hade kommit då och hette tryckkontroll. Vi hade problem med höga luftvägstryck, vi hade bara de volymkontrollerade moden och patienterna blev sjukare och sjukare och det blev svårare och svårare att kontrollera luftvägstrycket. I volymkontroll ställde vi in volymen, frekvensen och då fick vi det luftvägstryck vi fick. I tryckkontroll ställer vi luftvägstrycket och sedan frekvensen och så får vi den volym vi får. Vi blåser upp ett antal andetag upp till det tryck vi bestämmer, varefter vi ändrar flödesbilden. Det finns något som kallas fyrkantsandning. I de gamla respiratorerna såg de gamla flödesbilderna ut så, att när man blåste in ett andetag så accelererade man upp till ett topptryck, man hade en paustid på ca 10% v andetagsfasen, där man descellererade och sedan utandning. Detta ger extremt höga topptryck. När man uppfann tryckkontroll ändrade man på flödesbilden och gjorde max flöde från första sekunden och tills utandningen påbörjades. ”Pang på”, väldigt snabbt flöde, max hela vägen tills utandningen påbörjades. Det visade sig att man fick in mera luft på mindre tryck och därmed hade vi vunnit lite grand. Man hade t ex en patient som hade 55 cmH2O i luftvägstryck och som vi tyckte var för högt. Då bestämde vi att den patienten skulle ha 40 cmH2O i luftvägstryck och ställer in honom på det och får se vilken volym vi får. Oftast var volymen kanske lite lägre än vad vi hade i volymkontrollen, men vi hade fått ned trycket. Ville vi ha upp volymen kunde vi öka frekvensen lite grand. Vid volymkontroll har vi bestämt en volym, ökar man frekvensen delar man bara sönder kakan i mindre bitar, andetagen blir bara mindre men volymen är ju redan bestämd. Men när man har tryckkontroll har vi bestämt att man blåser upp ett andetag till det här trycket. Om vi blåser upp flera andetag per minut till det här trycket får vi givetvis en större volym. På det viset kommer man runt det hela. Då hade vi alltså en respirator med vars hjälp vi kunde sänka trycket något.
I och med att man började med invasiv ventilation var det också viktigt att man hade trachealkuber med cuff, så att man verkligen hade tätt. När vi körde små barn kunde man inte ha cuff, varför man fick läckage i volymkontrollen. Man pressade ned luften men det läckte hela tiden eftersom det inte var någon cuff. När man körde tryckkontroll tog man bort paustiden och blåste bara in-ut, in-ut, och då minimerade man läckage från de här barntuberna. Läckaget är minimalt när man kör tryckkontroll och man kan mäta det mesta, men kör man volymkontroll blir det en helt annan flödesbild med mycket större läckage som man inte kan mäta. Men alla vuxna patienter har alltså cuff och då kan man kontrollera det på ett helt annat sätt. Tryckkontroll är bra när man vill komma ner i luftvägstrycket. Den här respiratorn hade också en inhalator. Vi har en variant där vi kör 8 liter syrgas från väggen i en liten behållare och så inhalerar man kombivent.
En annan variant är att man lägger in de här burkarna på systemet och släpper in den fuktiga luften. Då går alla mätarna ”i taket”, Vi blåser in 8 liter i systemet och det följer med en tredjedel på varje inandning. Två tredjedelar går ut genom utandningssidan. Den här respiratorn ger en puff på varje andetag. När man kopplar apparaten till en inhalator känner den av vilken frekvens vi har på respiratorn och ger en puff på varje andetag. Det blir visserligen felvärden men det blir inte så stora flöden i slangarna och därmed inte så jobbigt för patienten.
Samtidigt som vi hade gamla Engströmarn fanns det också en Servo 900B. Vi använde inte den på intensivvårdsavdelningen. Vi hade den på operationsavdelningen. Innan vi köpte Servo 900C hände det att vi lånade in Servo 900B när vi hade ett litet barn. Den apparaten hade bara ett andningsmod också och det var volymkontroll precis som gamla Engströmarn. De här utvecklades runt 1959-60 och blev senare Servo 900C med tryckkontroll. Vi köpte tre Servo 900C, vilket var ett steg tillbaka. Vi hade fått Erika 1980 och när man skulle rengöra tog man bara ut plåtbyttan, slet sönder den i fem delar och slängde in i diskmaskin sedan var det klart. Servo 900C hade tryckkontroll och var modernare än Erika men när det gällde de här delarna upplevde personalen att den nya respiratorn var gammalmodigt, eftersom delarna skulle plockas isär, rengöras och läggas i diskmaskin, autoklaveras och flödesgivarna skulle läggas i sprit etc. Vi var tillbaks till gamla Engströmarns tid. Dessutom var det mycket knappar på Servo900C och det var mycket klagomål när vi köpte den. Det tog flera år innan ”personalen godkände dem”.
Ungefär samtidigt, ca 1984, kom fukt/värmeväxlare, passiva befuktningsfilter och även bakteriefilter som man kunde lägga på respiratorerna. Då behövde man inte rengöra dem lika ofta. Det var anledningen till att vi accepterade Servo 900C. När man hade en bakterie/virusfilter som man bytte var 24.e timma och skötte det behövde man bara rengöra respiratorn var tusende timma. Då kunde man köra på flera patienter.
Tiden mellan 1984-1990 provade vi en mängd olika befuktningsfilter och vi hade ett som kom från Engström som fungerade alldeles utmärkt men vi blev tvingade prova mycket annat. Först när vi återgick till ”edithnäsan” fungerade det igen. ”Edithnäsan” var alltså ett befuktningsfilter som man lade nära patienten och innehåller lite salt. Salt drar till sig vatten och när patienten andas ut varm fuktig utandningsluft kyls den ned, det blir dagg, som samlas i filtret. Eftersom det ligger salt i den här filtervävnaden drar den till sig extra mycket vatten och det blir mycket vått i filtret. När man skickade in torr andningsluft återfuktades filtret, patienten befuktade således sin egen luft. Detta fungerade dåligt i början, men edithnäsan har alltid fungerat bra, men produkter från andra firmor var inte lika bra. Vi kunde då få tubstopp, och ibland funderade vi på att använda aktiv befuktning, då man värmer upp med en apparat eller om vi skulle ha de här filtren. Men så återgick vi till de här näsorna som vi hade ända fram tills för några år sedan och som fungerat mycket bra. Då blev allting enklare. Vi hade ett bakterie/virusfilter som skyddade respiratorn och ett befuktningsfilter som vi bytte varje dygn och höll tuberna öppna. Tuberna är trachealtuber som patienterna andas genom och som går ner till lungorna. Ibland har vi tracheostomikanyler som går via halsen och in, i alla akutskeenden har vi trachealtuber, som går antingen via munnen eller näsan ner till trachea. Det blir lätt torrt i de här tuberna och om slemmet får bygga på sig blir det stopp.
Den 1 december 1995 köpte vi den första Servo 300.
Då tog respiratorutvecklingen ett stort steg framåt. Servo300 har något som kallas för flödestrigg. De gamla respiratorerna hade trycktrigg, vilket innebar att när patienten ville ta ett extra andetag eller inandningshjälp var han tvungen suga ett vakuum i slangpaketet fram till respiratorn på –2 cm vatten. Han måste suga ett vakuum för att respiratorn skulle känna att patienten behövde ett extra andetag eller inandningshjälp. När den här respiratorn kom hade den flödestrigg och då hade man svängt på det hela. Efter utandningen ger respiratorn ett litet flöde, två liter luft per minut blåser mot patienten hela tiden. Om patienten triggar, suger, det minsta lilla ökar flödeshastigheten och då känner respiratorn av det och puffar på inandningshjälp eller ett extra andetag eller vad vi har ställt in. Detta gjorde att alla de här gamla andningsmoden som vi har med oss från de gamla respiratorerna som även finns i den här blev som nya tack vare att det blev så lätt att andas extra andetag. Vi kan börjar träna ur patienterna mycket tidigare eftersom vi inte behöver suga så starkt innan vi får det extra andetaget. Urträning går bara lättare och lättare ju bättre respiratorer vi får.
När vi fick de här senaste respiratorerna kallade vi dem för Manhattan. Det var mängder av lampor som blinkade och tutade. Men så snart vi lärde oss använda den här respiratorn känns det tryggt att använda den. Det finns en guide. När en sjuksköterska eller en doktor skall ställa in ett nytt andningsmod trycker man på det andningsmod man skall ställa in blinkar en lampa på de knappar som man skall ställa in det här andningsmodet. De knappar som inte har med det här modet att göra de blinkar inte. Man går med den här guiden runt hela apparaten och då vet man att man inte missar en enda knapp.
Nytt på den här respiratorn var VKTS (volymkontrollerad tryckstyrning). De fungerar så att vi ställer in den volym och den frekvens som vi vill att patienten skall andas. Respirator ställer automatiskt in de luftvägstryck som behövs för att skjuta in den föreskrivna volymen. Om tryckföhållandena förändras under behandlingens gång, till exempel att patienten vänder sig på sida, så att de börjar gå tyngre att blåsa ner andetagen. Då märker respiratorn de och ökar inblåsnings trycket med 3cmH2O tills den når den nivå som erfordras för att blåsa ned andetaget på denna unika patient. Om patienten däremot vänder sig på rygg vilket gör att de plötsligt går mycket lättare att andas då märker respiratorn de och sänker inblåsningstrycket med 3cmH2O i taget tills vi är ner på den nivå som är aktuell för tillfället.
Vi har alltså fått en respirator som automatiskt ger varenda andetag till lägsta möjliga luftvägstryck.
Det finns också en version av inandningshjälp. Gamla inandningshjälpen var detsamma som tryckunderstöd på Servo 900C och även på den här senaste. Det finns också något som heter volymunderstöd som är intimt sammankopplat med VKTS. Om man tycker att patienten börjar andas själv, drar ett antal spontanandetag varje minut, och det är dags att patienten får andas lite själv, kan vi vrida över till volymunderstöd. Respiratorn vet referensvärdena från VKTS och vet att den här volymen skall patienten andas och den här frekvensen. Om patienten orkar andas den här volymen och hålla den här frekvensen då ger respiratorn bara blandad syrgas och luft. Efter fem timmar kanske patienten börjar ”krokna” och volymerna förändras och då märker den att för att hålla volymen börjar den skjuta på. Patienten behöver bara trigga igång andetaget så får han hjälp upp till de volymer vi har ställt in. Om patienten blir så trött att han inte orkar trigga igång ett andetag utan får apné går det 20 sekunder, varefter respiratorn automatiskt hoppar över kontrollerad mode i VKTS och tar över andningen.
Vi gjorde en uppdatering år 2000 till Servo 300A. Då kom något som hette automode. Då hade respiratorn automatiserats ytterligare. Den hjälper oss vid urträning av patienter ur respirator VKTS och volymunderstöd finns fortfarande men ytterligare en ruta har tillkommit, en automode ”till”. När vi har automode ”till” fungerar det automatiskt. Automode går att koppla in på ett antal kontrollerade andningsformer och sammanbinder spontanandningsmodena med de kontrollerade formerna av andningsmode. Patienten ligger VKTS i kontrollerat mode. När patienten är så pigg att han börjar andas två spontana andetag efter varandra hoppar respiratorn automatiskt över i volymunderstöd, vilket betyder att patienten måste andas varje andetag själv, Behöver patienten hjälp får han det upp till de referensvärden vi har ställt in. Tar patienten en paus på 12 sekunder får apné, då hoppar apparaten tillbaka till kontrollerat mode. Detta fungerar emellertid inte så bra om man sätter på för tidigt. Patienten skall vara ganska vaken och duktig på att andas för att det skall fungera så bra att värdena kan hoppa emellan. Ofta är det så att vi väntar så länge att när patienten börjar spontanandas vrider vi över till automode och när den hoppar över till volymunderstöd ligger den kvar där tills vi kan koppla ur.
Ovanför respiratorn sitter en liten dataskärm, det är mest lyx, men det finns två loopar, flöde/volymloopen som man kan titta på och se hur obstruktiv patienten är. Man kan mäta lite autopeep eller totalpeep. Om man har ställt in ett IE-förhållande som inte är riktigt bra: En astmatiker har svårt att andas ut och klarar sig sällan på ett normalt ie-förhållande. Om man har ett normalt ie-förhållande på 1-2 och lägger en astmatiker i respiratorn så säger den att den inte hinner andas ut innan den får nästa andetag. Då bygger vi upp ett högt tryck i bröstkorgen och det är autopeep. Man kan mäta det här totalpeepet på servoscreenen och se att den här patienten har ett för högt intratrocaltryck Vi behöver förlänga utandningstiden så att patienten kanske skall ligga på ett ie-förhållande 1-3, då känner respiratorn att det här är normalt för en astmatiker. Patienten hinner andas ut innan nästa andetag kommer.
I dagens respiratorer har man bara tagit med två loopar från servoscreenen. Det är de viktigaste flödevolymen och tryckvolymen, som vi har med i den här allra nyaste servoI.
Idag på intensivvårdsavdelningen finns pendlar som hänger ned från taket, en AGA-pendel. Varje AGA-pendel kostar 100 000 kr. Vi har ett övervakningssystem som heter HP, där vi kan övervaka blodtryck, puls, centralt ventryck, mäta syresättning m m på en dataskärm överst, därunder har vi själva respiratorn och sedan syrgasapparater, pumpar osv. Det vi vinner med det här är att vi har allt på ett ställe och allt kommer därifrån direkt till sängen. Vi har möjlighet att kunna gå runt sängen, vi kan stå ovanför patienten och suga slem, stå på sidorna och bädda. Skillnad mot förr då vi hade alla apparater på en panel bakom sängen och alla sladdar gick som i en solfjäder och man kom inte åt patienten. Vi har även lagt sängarna lite snett för att komma åt bättre och tagit bort hyllor för att få in respiratorn under. Meningen är att utrymmet runt sängen skall vara fritt. Lyftar i taket så att vi kan lyfta våra patienter, vilket är bra då vi har hög medelvikt på våra patienter idag. Lyftarna tar 170 kg och vi har haft några patienter där lyftarna inte har orkat med.
Den allra senaste respiratorn heter Servo I. Det är bara en liten dataskärm, utandningssida. Det är exakt samma apparat som Servo 300a bortsett från att alla funktioner har kopplats in i dataskärmen och respiratorn är något smäckrare till utformningen, står som på en stolpe. Den är utrustad med en expirationskassett som man med ett snäpp kopplar bort och slänger in i diskmaskin, kopplar på en silikonslang som sprutar igenom 85-gradigt vatten i tio minuter, varefter den är diskad. Kassetten torkas i ett torkskåp, varefter den täthetstestas och det är klart för att köra inom fem minuter på nästa patient. Den här respiratorn täthetstestar sig själv. Det är bara att trycka igång, efter tre minuter har den gått igenom hela programmet och startar sedan upp. Vi står bara bredvid och tittar och godkänner. De andra lite äldre respiratorerna tar ca 20 minuter för en van att täthetstesta, för en ovan ca en timma. Det går framåt hela tiden.
Den här respiratorn har ett mycket bättre automode än vad Servo 300a har. Vi hade en dam som man hade lagt på automode för tidigt i den här Servo 300a. Damen hade legat och vilat i respiratorn, vaknat upp och kände sig pigg och orkade andas två spontana andetag när hon stod i automode. Då hoppade den över till volymunderstöd, därefter somnade hon. Efter 12 sekunder gick det ett larm att det var för lågt utandningsvolym. Då vaknade damen till och apparaten hoppade till ett kontrollerat andetag. Då drog hon två spontana andetag och hoppade över i volymunderstöd och så somnade damen. Så gick det 12 sekunder och så höll det på. Vi hade alltså lagt henne för tidigt i automode. Detta kan aldrig hända i servoI. Man har 7 sekunder apnétid uppdelad i tio spontana andetag, vilket betyder att om patienten ligger i kontrollerat mode i VKTS satt på automode och patienten bara drar ett spontant andetag, det första andetaget är 3 sek långt, det är 4 sek kvar, vilket delas upp i tiondelar. Om patienten andas tio spontana andetag efter varandra har de 7 sek i apnétid men om patienten bara andas det ordinarie andetaget och ett spontant andetag har han 3,8 sek apnétid. Det betyder att om patienten inte snabbt nog tar ett nytt spontant andetag hoppar det genast över i kontrollerat mode igen. Man ser på ServoI att det hoppar hela tiden över i volymunderstöd, kontrollerat, volymunderstöd, kontrollerat. Först när patienten orkar andas tio spontana andetag efter varandra har de 7 sek apnétid innan den hoppar tillbaka och det betyder att patienten kan vara lite unik i sin andning, ta lite småpauser, behöver inte gå som en maskin och fortfarande kunna ligga kvar i spontanandning. Man kan alltså lägga en fullt nedsövd patient i ett kontrollerat mode och lägga på automatmode från början. När patienten blir pigg och vaken och kan andas ett spontant andetag är respiratorn med och hjälper till. Respiratorn tränar ur patienterna kan man säga. Det börjar luta åt det hållet.
Sedan några år tillbaka har vi fått möjlighet att köra Maskandning via respirator på KOL patienter och astmatiker. De är ett mycket populärt sätt att använda respiratorns funktioner utan att behöva lägga ner en tub i andningsvägarna och de trauma som detta medför.
Patienten kommer till IVA och inte klarar sin egen andning. Vi placerar då en mask på ansiktet som vi spänner fast med en hätta på huvudet. Kopplar till respiratorn och ställer den på en funktion som heter Tryckunderstöd+Cpap. Patienten måste hela tiden fortsätta att spontan andas men får för varje andetag en puff av respiratorn som vi bestämmer storleken på. Vi blåser även upp andningsvägarna med Peep tryck som vi pratade om tidigare. Cpap är bara ett annat ord för samma sak. Många patienter klarar vi idag på det här viset utan att lägga dem i respirator. Tyvärr är de så att största delen av våra patienter fortfarande måste intuberas och läggs i respirator.
2000-talet har medfört att vi fått möjlighet att köpa in två av de nyaste och bästa respiratorerna som finns på marknaden idag Servo i heter den De är i stort samma respirator som Serv300A men den är bara lite förfinad smidigare lättare att rengöra och tar mindre plats.
Rengöringen går till så att man tar ut utandningskassetten kör den i diskmaskin och låter den torka i två timmar. Vi har extra utandningskassetter som gör att vi kan starta respirator på nästa patient inom 5min, från de vi har avslutat föregående patient.
Automodet på Servo i är mycket bättre och fungerar på ett smidigare sätt för patienten vilket gör att ur träningarna sällan är ett problem idag.
Kostnader på Intensivvårdsavdelningen år 2003
Dygnskostnaden på IVA idag/patient är ca 15300 kr. De är för den absolut enklaste patienten som ligger uppkopplad med EKG övervakning Puls och blodtryck och extravak + Sjuksköterska och doktor tillgängliga.
Aga pendeln kostar ungefär 100000 kr st,
Övervaknings apparaturen som mäter blodtryck EKG Syresättning med mera kostar ca 200000 kr st.
De nyaste ventilatorerna som vi just inhandlat kostar ca 320000 kr st.
Läkemedelskostnaderna på IVA och Postop är Ca 300000 kr /månad.
Nya IVA sängar kostar ca 27000 kr/st
Två nya Decubitusmadrasser kostar ca 45000 kr/st.
De här är något av våra kostnader och vittnar om att sjukvård är väldigt dyrt.